Introducción
Eicosanoides
Les comparto un vídeo sobre los líquidos eicosanoides de forma sencilla: Liquidos eicosanoides.
Biosíntesis
La biosíntesis de eicosanoides está limitada por la
disponibilidad de AA y depende principalmente de la liberación de AA
esterificado de los fosfolípidos de membrana u otros lípidos complejos por
acilhidrolasas, especialmente PLA2. Una vez liberado, el AA se metaboliza
rápidamente a productos oxigenados por COX, LOX y CYP.
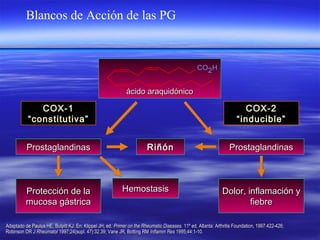
Productos de ciclooxigenasas (sintasas de prostaglandina
G/H)
La prostaglandina endoperóxido G/H sintasa se llama
ciclooxigenasa o COX coloquialmente. Los productos de esta vía son PG, PGI2 y
TxA2, denominados en su conjunto prostanoides.
Los prostanoides se distinguen por sustituciones en sus anillos de
ciclopentano del número de dobles enlaces en sus cadenas laterales, como lo
indican los subíndices numéricos.
Productos de las lipoxigenasas
Los principales productos de las vías LOX son los derivados
de ácidos grasos hidróxidos conocidos como HETE, LT, y LX. Los LT juegan un
papel fundamental en el desarrollo y persistencia de la respuesta inflamatoria.
Las LOX son una familia de enzimas que contienen hierro no hemático; las LOX
catalizan la oxigenación de ácidos grasos poliénicos en los correspondientes
lípidos hidroperóxidos.
Productos de CYP
Las epoxigenasas CYP, principalmente CYP2C y CYP2J
metabolizan el AA en EET. En las células endoteliales los EET funcionan como
EDHF, particularmente en la circulación coronaria. La biosíntesis se altera por
factores genéticos, nutricionales y farmacológicos, que afectan la expresión de
CYP.
Inhibidores de la biosíntesis de los eicosanoides
La inhibición de PLA2 disminuye la liberación del ácido
graso precursor y la síntesis de todos sus metabolitos. Las PLA2 pueden ser
inhibidas por fármacos que reduzcan la accesibilidad de Ca²+. Los
glucocorticoides inhiben la PLA2 indirectamente al inducir la síntesis de un
grupo de proteínas llamadas anexinas que modulan la actividad de PLA2. Los
glucocorticoides también regulan la disminución de la expresión inducida de
COX-2 pero no de COX-1.
Degradación de los eicosanoides
La mayoría de los eicosanoides son inactivados rápida y
eficientemente. Las reacciones catabólicas enzimáticas son de dos tipos:
• Un paso inicial rápido, catalizado por enzimas PG
específicas ampliamente distribuidas, en el que las PG pierden la mayoría de su
actividad biológica.
• Un segundo paso en el que estos metabolitos se oxidan,
probablemente por enzimas idénticas a aquellas responsables de la oxidación β y
ω de los ácidos grasos.
El pulmón, el riñón y el hígado juegan papeles destacados en las reacciones catalizadas enzimáticamente.
Propiedades farmacológicas
Los eicosanoides funcionan a través de GPCR específicos que
se acoplan a los sistemas de segundo mensajero intracelulares para modular la
actividad celular.
Receptores de prostaglandina
Las PG activan receptores de membrana localmente cerca de
sus lugares de formación. Los receptores de eicosanol interactúan con Gs, Gi y
Gq para modular las actividades de adenilil ciclasa y PLC. Los productos de un
solo gen han sido identificados por los receptores de PGI2, PGF2α y TxA2.
Cuatro diferentes receptores PGE2 (EP1-4) y dos receptores PGD2 (DP1 y DP2) han
sido clonados.
Receptores leucotrienos
Existen dos receptores para LTB4 (BLT1 y BLT2) y CysLT1 y
CysLT2. El receptor fMLP-2 también se une a LXA4, pero la importancia funcional
de este ligando in vivo todavía es controvertida. Todos son GPCR y combinan con
Gq y otras proteínas G, en dependencia del contexto celular. La BLT1 se expresa
predominantemente en los leucocitos, el timo y el bazo, mientras que BLT2, el
receptor de baja afinidad para LBT4, se encuentra en el bazo, los leucocitos,
el ovario, el hígado y el intestino.
Acciones fisiológicas y efectos farmacológicos
La amplia biosíntesis y múltiples acciones farmacológicas de
los eicosanoides se reflejan en su compleja fisiología y fisiopatología. El
conocimiento de la distribución de los principales receptores eicosanoides
ayuda a poner en perspectiva esta complejidad.
Sistema cardiovascular
Debido a su corta t1/2, los prostanoides actúan localmente y por lo general se considera que no afectan el tono sistémico vascular en forma directa. Pueden modular el tono vascular localmente en sus sitios de biosíntesis o a través de efectos renales u otros efectos indirectos. La PGI2, el metabolito araquidonato más importante liberado del endotelio vascular se deriva en primera instancia de COX-2 en sereshumano.
Plaquetas
Inflamación e inmunidad
Los eicosanoides tienen un papel importante en las
respuestas inflamatorias e inmunes. Por lo general los LT son proinflamatorios
e interactúan con las PG para promover y mantener la inflamación, aunque hay
algunas excepciones, como las acciones inhibitorias de PGE2 en la mayoría de la
activación de los mastocitos.
El músculo bronquial y traqueal
Una mezcla compleja de autacoides se libera cuando el tejido
del pulmón sensibilizado es afrontado por el antígeno apropiado, incluyendo el
broncodilatador derivado de COX y sustancias constrictoras de los bronquios.
Entre estas, la TxA2, la PGF2α y la PGD2 contraen, y la PGE2 y la PGI2 relajan
el músculo bronquial y traqueal.
Aproximadamente 10% de las personas a las que se administra
ácido acetilsalicílico o NSAID desarrolla broncoespasmos.
Músculo liso GI
Las prostaglandinas E2 y PGF2 estimulan la contracción del
músculo longitudinal principal del estómago y el colon. Los endoperóxidos PG,
TxA2, PGI2 también producen contracción, pero son menos activos. El músculo
circular generalmente se relaja en respuesta a la PGE2 y se contrae en
respuesta a PGF2α. Los LT tienen potentes efectos contráctiles.
Se han observado diarreas, calambres y reflujo de la bilis
en respuesta al PGE oral. Los PGE y PGF estimulan el movimiento del agua y los
electrolitos en la cavidad intestinal.
Secreción GI
La PGE2 y la PGI2 contribuyen, en el estómago, al incremento
de la secreción de mucus, a la secreción reducida de ácido y del contenido de
pepsina. La PGE2 y sus análogos también inhiben el daño gástrico causado por
una variedad de agentes ulcerogénicos y promueven la cura de las úlceras
gástricas y duodenales.
Útero
Riñón
Los productos derivados de la COX promueven la excreción de
la sal en los conductos recolectores. Las PGE2 y PGI2 derivadas del COX-2
cortical aumentan el flujo sanguíneo renal y la filtración glomerular a través
de sus efectos vasodilatadores locales y como parte del mecanismo de
retroalimentación tubuloglomerular que controla la liberación de renina.
Ojo
La prostaglandina F2α provoca la constricción del músculo
del esfínter del iris, pero su efecto global en el ojo es disminuir la presión
intraocular al incrementar la salida de humor acuoso. Una variedad de agonistas
de FP ha demostrado ser efectivos en el tratamiento del glaucoma de ángulo
abierto, una condición asociada con la pérdida de la expresión de COX-2 en el
epitelio pigmentado del cuerpo ciliar.
Sistema nervioso central
La prostaglandina E2 produce fiebre. El hipotálamo regula el
nivel normal de la temperatura corporal, que se eleva por pirógenos endógenos
como el IL-1β, IL-6, TNF-α e interferones. La respuesta está mediada por la
inducción coordinada de COX-2 y mPGES-1 en el endotelio de los vasos sanguíneos
en el área hipotalámica preóptica para formar PGE2.
Dolor
Los mediadores inflamatorios, que incluyen LT y PG, aumentan
la sensibilidad a los nociceptores y potencian la percepción del dolor.
Centralmente, COX-1 y COX-2 están expresados en la columna vertebral bajo
condiciones basales y liberan PG en respuesta a estímulos dolorosos
periféricos. Tanto la PGE2, a través de los EP1 y EP4, como la PGI2, vía los
IP, reducen el umbral de la estimulación de nociceptores.
Sistema endocrino
La administración sistémica de PGE2 aumenta las
concentraciones de circulación de ACTH, la hormona del crecimiento, la
prolactina y las gonadotropinas.
Hueso
Las prostaglandinas son moduladores potentes del metabolismo
óseo. COX-1 se expresa en el hueso sano, mientras que COX-2 es regulada en
escenarios como la inflamación y durante la tensión mecánica. La PGE2 estimula
la formación de hueso al incrementar la osteoblasto génesis y la resorción ósea
vía activación de osteoclastos.
Cáncer
La inhibición
farmacológica o eliminación genética de COX-2 refrena la formación de tumores
en modelos de colon, mama, pulmón y otros cánceres. La PGE2 ha sido implicada
como el prostanoide pro oncogénico primario en múltiples estudios.
Usos
terapéuticos
Inhibidores y antagonistas
Los NSAID son muy usados como fármacos antiinflamatorios,
mientras que el ácido acetilsalicílico en dosis bajas se emplea frecuentemente
para el cardio protección.
Los antagonistas de LT son clínicamente útiles en el
tratamiento del asma, y los de FP se usan para tratar el glaucoma de ángulo
abierto.
Los agonistas de EP son útiles para inducir el trabajo de
parto y para aliviar la irritación gástrica debido a los NSAID. Los
antagonistas de DP1 podrían ser útiles para suprimir el rubor facial asociado
con el niacina.
Los prostanoides tienen una corta t1/2 en la circulación, y
su administración sistemática produce efectos adversos significativos. Sin
embargo, varios prostanoides son de utilidad clínica en las siguientes
situaciones.
Trabajo de parto y aborto terapéutico: las
prostaglandinas E2, PGF2α y sus análogos se utilizan para inducir el trabajo de
parto a término y poner fin al embarazo en cualquier etapa al promover las
contracciones uterinas. Sus agentes facilitan la labor de parto al promover la
maduración y dilatación del cérvix. Se utilizan dinoprostona e misoprosol.
Mantenimiento del conducto arterioso persistente:
mantener un conducto persistente puede ser termodinámicamente importante en
algunos recién nacidos con enfermedad cardiaca congénita. El PGE1 es altamente
efectivo para terapia paliativa para mantener la evidencia temporal hasta que
se pueda realizar la cirugía.
Citoprotección gástrica: varios análogos de PG se
utilizan para suprimir la ulceración gástrica. El misoprostol, un análogo de
PGE1, está aprobado para la prevención de úlceras gástricas inducidas por NSAID
y es casi tan efectivo como el inhibidor de bomba de protones omeprazol.
Impotencia: la prostaglandina E1, suministrado como
inyección intracavernosa o supositorio uretral, es un tratamiento de segunda
línea para la disfunción eréctil. Los inhibidores fosfodiesterasa 5 han
sustituido al PGE1 como el tratamiento preferido para esta condición.
Factor
activador de plaquetas
Química
Sitios de síntesis del PAF
El factor activador de plaquetas no se almacena en las células, sino que se sintetiza en respuesta a la estimulación. El PAF se sintetiza mediante plaquetas, neutrófilos, monocitos, mastocitos, eosinófilos, células mesangiales renales, células medulares renales y células endoteliales vasculares.
Mecanismo de acción del PAF
El PAF extracelular ejerce su acción al estimular un GPCR
específico. El receptor de PAF se acopla a Gq para activar la vía de
PLC-IP3-Ca2+ y a Gi para inhibir la adenilil ciclasa. La activación consecuente
de los PLA2, C y D dan lugar a segundos mensajeros, que incluyen PGs, TxA2 o LT
derivados de AA, que pueden funcionar como mediadores de los efectos de PAF.
Funciones fisiológicas y patológicas del PAF: El
factor activador de plaquetas suele considerarse como un mediador de eventos
patológicos y se le ha implicado en el asma alérgica, choque endotóxico,
pancreatitis aguda, ciertos cánceres, inflamación dérmica y enfermedades
cardiovasculares inflamatorias tales como aterosclerosis.
Respuestas inflamatorias y alérgicas: La
administración experimental de PAF reproduce muchos de los signos y síntomas en
el choque anafiláctico, los efectos de los antagonistas de PAF en el
tratamiento de trastornos inflamatorios y alérgicos han sido decepcionantes. En
pacientes con asma, los antagonistas de PAF inhiben parcialmente la
broncoconstricción inducida por la exposición al antígeno.
Sistema cardiovascular: El factor activador de
plaquetas es un vasodilatador potente en la mayoría de los lechos vasculares;
cuando se administra por vía intravenosa, causa hipotensión. La vasodilatación
inducida por PAF es independiente de los efectos sobre la inervación simpática,
el sistema renina-angiotensina o el metabolismo de AA, y probablemente sea el
resultado de una combinación de acciones directas e indirectas.
Plaquetas: el receptor de PAF se expresa de manera
constitutiva en la superficie de las plaquetas. El PAF estimula con potencia la
agregación de plaquetas. La inyección intravenosa de PAF causa la formación de
agregados plaquetarios intravasculares y trombocitopenia
Leucocitos: El factor activador de plaquetas es un
potente y común activador de células inflamatorias. El PAF estimula una
variedad de respuestas en PMN. Estimula los PMN para agregar, desgranular y
generar radicales libres y LT.
Músculo liso: El factor activador de plaquetas
contrae el músculo liso GI, uterino y pulmonar. El PAF aumenta la amplitud de
las contracciones uterinas espontáneas; estas contracciones son inhibidas por
inhibidores de la síntesis de PG. El PAF no afecta el músculo liso traqueal,
pero produce contracción del músculo liso de las vías respiratorias.
Estómago: además de contraer el fondo del estómago,
el PAF es el más potente ulcerógeno conocido. Cuando se administra por vía
intravenosa, causa erosiones hemorrágicas de la mucosa gástrica que se
extienden hacia la submucosa.
Riñón: el factor activador de plaquetas disminuye el flujo sanguíneo renal, la tasa de filtración glomerular, el volumen urinario y la excreción de Na+ sin cambios en la hemodinámica sistémica. El PAF ejerce un efecto bifásico mediado por el receptor sobre las arteriolas aferentes, las dilata en concentraciones bajas y las contrae en concentraciones más altas.
Bibliografía
Goodman &
Gilman. Las Bases Farmacológicas de la
Terapéutica Ed.13
Autores: , Björn C. Knollman





Me parece un tema bastante interesante
ResponderEliminarLos temas me paresen muy interesantes
EliminarMuy Interesante
ResponderEliminarExcelente información de mucha utilidad
ResponderEliminarQue bueno saber sobre este tema
ResponderEliminar